2025 markiert einen wesentlichen Fortschritt in der Behandlung der Demenz vom Alzheimertyp in Österreich: mit Donanemab und Lecanemab wurden zwei spezifische, also speziell gegen den Krankheitsmechanismus gerichtete, Therapien in Österreich zugelassen. Doch nicht jeder Patient/jede Patientin ist dafür geeignet. In diesem Artikel wollen wir Ihnen die Details vorstellen.
URSACHEN DER ALZHEIMER-DEMENZ
In der Entstehung der Alzheimer-Demenz sind nach derzeitigem Verständnis vor allem die Ablagerung zweier Proteine im Gehirn verantwortlich.
Amyloidplaques
Einerseits das Amyloid-beta, das in Form von Verklumpungen zwischen den Nervenzellen zu liegen kommt, die Amyloidplaques genannt werden. Dies scheint die Kommunikation zwischen den Nervenzellen und auch die Versorgung mit Nährstoffen zu stören, was zu einem Absterben der Zellen führt. Anfangs lagern sich diese vor allem in einer Region namens Hippocampus ab, die für das Gedächtnis verantwortlich ist. Deshalb wird dieses meist als erstes auffällig.
Tau-Fibrillen
Das zweite Protein ist das Tau-Protein. Dies ist im inneren der Nervenzelle und sorgt für Stabilität und Versorgung mit Nährstoffen. Bei der Alzheimer Demenz wird es so verändert, dass es sich fadenförmig als sogenannten Tau-Fibrillen im inneren der Zelle ablagert. Dadurch verliert die Zelle Form und Funktion und stirbt ab.
Momentane neue Entwicklungen auf dem Gebiet der Therapie setzen vor am Amyloid an.
ANTIKÖRPERTHERAPIE BEI DEMENZ
Wirkmechanismus der neuen Therapien
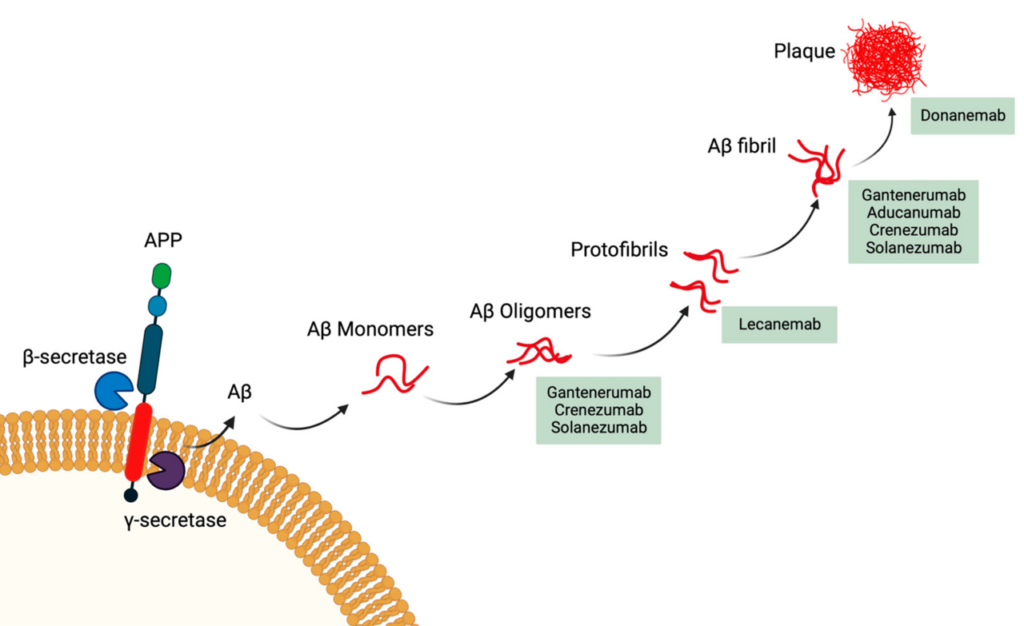
Amyloid-beta kommt normalerweise im Gehirn vor und trägt zur normalen Funktion bei. Bei der Alzheimer-Erkrankung verklumpt es zunächst zu sogenannten Oligomeren, von denen sich mehrere zu Fibrillen zusammenlagern. Diese bewegen sich noch innerhalb des Gehirns und verursachen bereits dadurch Schäden. Lagern sich dann mehrere Oligomere zusammen, entsteht ein großer, unbeweglicher Plaque, der die Gehirnzellen in seinem Umfeld absterben lässt.
Die beiden neuen Therapien sind Antikörper, die sich gegen unterschiedliche Stadien des Amyloids richten: Lecanemab setzt bei den Fibrillen an, Donanemab bei den Plaques. Die Antikörper binden an das Amyloid und markieren sie auf diesem Wege für unser Immunsystem. Nun als fremd erkannt, beginnt unser Immunsystem das Amyloid abzubauen.
Wirkstärke der Antikörpertherapie
Das Amyloid wird sehr effektiv aus dem Gehirn entfernt. Trotzdem darf man keine Heilung der Erkrankung erwarten, da viele Schäden ja bereits eingetreten sind. Was aber erzielt werden kann, ist eine Verlangsamung des Fortschreitens der Demenz. Das Ausmaß liegt bei etwa 30% Verlangsamung.
Wer ist für die Antikörper-Therapie geeignet?
Die Therapie ist für ein frühes Stadium der Alzheimer-Erkrankung zugelassen. Die Erkrankung darf also noch nicht zu weit fortgeschritten sein. Für die Eignung sind ausführliche Voruntersuchungen notwendig. Dies hängt damit zusammen, dass einerseits zunächst bewiesen werden muss, dass es sich bei der Demenz um eine Alzheimer-Demenz handelt. Andererseits muss man vorab ausschließen, dass die zu behandelnde Person ein erhöhtes Risiko für möglicherweise gefährliche Nebenwirkungen hat. So darf man zum Beispiel keine frühere Hirnblutung gehabt haben oder blutverdünnende Medikamente einnehmen. Ein Teil dieser Abklärung erfolgt über Hausarzt/Hausärztin, ein Teil bei Facharzt/Fachärztin für Neurologie oder Psychiatrie. Der Facharzt/die Fachärztin wird Sie dann gegebenenfalls an ein behandelndes Zentrum weiterüberweisen.

Wie läuft die Antikörper-Therapie ab?
Die Therapie wird als Infusion verabreicht und erfolgt derzeit ausschließlich an spezialisierten Zentren. Für Oberösterreich ist dies der Neuromed Campus des Kepler Universitätsklinikums. Dorthin werden Sie vom behandelnden Facharzt überwiesen, wenn die Voraussetzungen für eine Antikörper-Therapie – soweit im niedergelassenen Bereich abgrenzbar – gegeben sind. Wenn Sie sich für die Therapie entscheiden, bedeutet das, dass sie alle 2 Wochen bei Donanemab oder alle 4 Wochen bei Lecanemab über einen Zeitraum von zumindest zwei Jahre für einige Stunden im Krankenhaus sind. Auch sind regelmäßige MRTs des Schädels notwendig, um sich entwickelnde Nebenwirkungen früh zu erkennen. Im ersten Jahr zumindest vier.
Welche Nebenwirkungen sind möglich?
Zumeist wird die Therapie gut vertragen. Die häufigsten Nebenwirkungen sind Rötungen oder Schmerzen an der Einstichstelle der Infusion. Selten kann es zu allergischen Reaktionen kommen – was der Grund ist, warum man vor allem nach den ersten Infusionen noch einige Stunden im Krankenhaus überwacht wird.
Eine weitere wichtige Gruppe von seltenen Nebenwirkungen sind eine Schwellung des Gehirns oder kleine Blutungen. Man glaubt, dass es dazu kommt, weil das Amyloid eben abtransportiert wird. Zumeist verlaufen diese unbemerkt – was der Grund ist, warum das MRT des Schädels häufig wiederholt wird.
Wie soll ich vorgehen, wenn ich glaube, eine Demenz zu haben?
Ihr erster Weg ist zum Hausarzt. Dort sollte zunächst überprüft werden ob tatsächlich eine vermehrte Vergesslichkeit vorliegt – über Gespräch und erste orientierende Tests – und andere Ursachen wie zum Beispiel eine Schilddrüsenunterfunktion ausgeschlossen werden. Bei entsprechenden Auffälligkeiten werden Sie an Facharzt/ärztin für Neurologie oder Facharzt/ärztin für Psychiatrie überwiesen. Nach Gespräch und körperlicher Untersuchung werden die weiteren notwendigen Untersuchungen veranlasst.
In der Neurowerkstatt Gallneukirchen/Linz stehen wir Ihnen für die entsprechende Abklärung gerne zur Verfügung.
Weitere Informationen zum Nachlesen finden Sie unter: alzheimer-gesellschaft.at

Hereditäre Myopathien
Die häufigsten Erkrankungen aus diesem Spektrum sind die Myotone Dystrophie Typ 1 (DM1) auch Curschmann-Steinert-Erkrankung genannt und die Facioscapulohumerale Muskeldystrophie kurz FSHD. Die häufigste erbliche Myopathie im Kleinkindalter ist die Muskeldystrophie Duchenne welche allerdings nur bei Knaben auftritt. Eine abgeschwächte Form dieser Erkrankung kann bei Männern im jüngeren Erwachsenenalter auftreten und wird dann als Muskeldystrophie Becker bezeichnet. Die Diagnose wird mittels kommerzieller Gentests bestätigt.
Andere hereditäre Myopathien sind deutlich seltener und treten ebenfalls meist in jungen Jahren auf. Aufgrund der Seltenheit und der oft unspezifischen klinischen Phänomenologie erfolgt die Diagnosestellung fast immer mittels Genetik durch spezielle Panels oder ein Whole Exome Sequencing.
Im späteren Erwachsenenalter können sich zB die myofibrillären Myopathien oder die Myotone Dystrophie Typ 2, auch PROMM (proximale myotone Myopathie) genannt, erstmalig bemerkbar machen. Auch bei diesen sind die klinische Untersuchung und eine EMG/ENG-Untersuchung erforderlich. Ein nachfolgender Gentest bestätigt die Diagnose.
Eine ursächliche Therapie ist bei genetisch bedingten Muskelerkrankungen derzeit nur bedingt möglich. Für die Duchenne Muskeldystrophie sind aber symptomatische Behandlungen und für bestimmte Gen-Mutationen bereits Gentherapien verfügbar welche das defekte Dystrophin zumindest teilweise wieder verfügbar machen. Bei der DM1 und FSHD sind vielversprechende Therapien in einem fortgeschrittenem Entwicklungsstadium, erste Studien sind kurz vor Abschluss.

Metabolische Myopathien
Stoffwechselbedingte Muskelerkrankungen treten überwiegend im Kindesalter oder jungen Erwachsenenalter auf wie zB die McArdle Erkrankung. Meist handelt es sich um Defekte im Zucker- oder Fettstoffwechsel der Muskelzellen, manchmal können auch Erkrankungen der Schilddrüse und zwar sowohl eine ausgeprägte Überfunktion (Hyperthyreose) als auch eine erhebliche Unterfunktion (Hypothyreose) eine Muskelschwäche auslösen.
Der Morbus Pompe, eine Glycogenose mit Störung im Glykogenstoffwechsel mit Mangel eines bestimmten Enzyms für den Abbau von Glykogen (Glucosidase Alpha), kann sich auch erst im höheren Lebensalter bemerkbar machen mit Problemen beim Stiegensteigen und manchmal isolierter Atemmuskelschwäche. Einschränkungen im muskulären Fettstoffwechsel (Lipidmyopathien) oder Erkrankungen der Mitochondrien (Mitochondriale Myopathien) können erst im Erwachsenenalter auftreten. Symptome treten charakterischerweise bei Belastung auf. Die Diagnose von metabolischen Myopathien erfolgt durch Detektion des Enzymmangels im Blut mittels Trockenbluttest und wird durch einen Gentest bestätigt. Beim Morbus Pompe kann bei frühzeitiger Diagnose eine Enzymersatztherapie das Fortschreiten verhindern bzw. für einige Zeit sogar zu einer merkbaren Verbesserung führen. Bei anderen Stoffwechselstörungen sind spezielle Diäten bzw. eine angepasste Ernährung erforderlich.
Hat man früher von Muskeltraining bei Myopathien abgeraten hat sich mittlerweile durch eine Vielzahl an durchgeführten Studien die Erkenntnis durchgesetzt, dass in nahezu allen Fällen ein regelmäßiges speziell angepasstes Krafttraining bei Muskelerkrankungen nicht nur möglich ist, sondern sogar empfohlen werden kann. Durch eine konsequente Trainingstherapie ist fast immer eine deutliche Verbesserung von Kraft und muskulärer Belastbarkeit möglich.
Da sowohl entzündliche als auch metabolische Myopathien immer besser behandelbar werden ist eine frühzeitige Diagnose sinnvoll um irreversible Schäden zu vermeiden. Die Neurologin/der Neurologe ist Spezialist für die Abklärung von Muskelerkrankungen und weiterführende Therapien.

Buchen Sie jetzt Ihren Termin:
Tel.: 07235 63884
Montag – Freitag 8:00 – 18:00 Uhr
oder einfach & schnell zum Termin online: